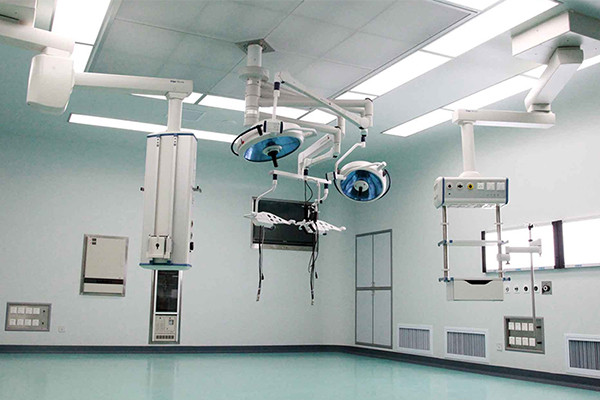
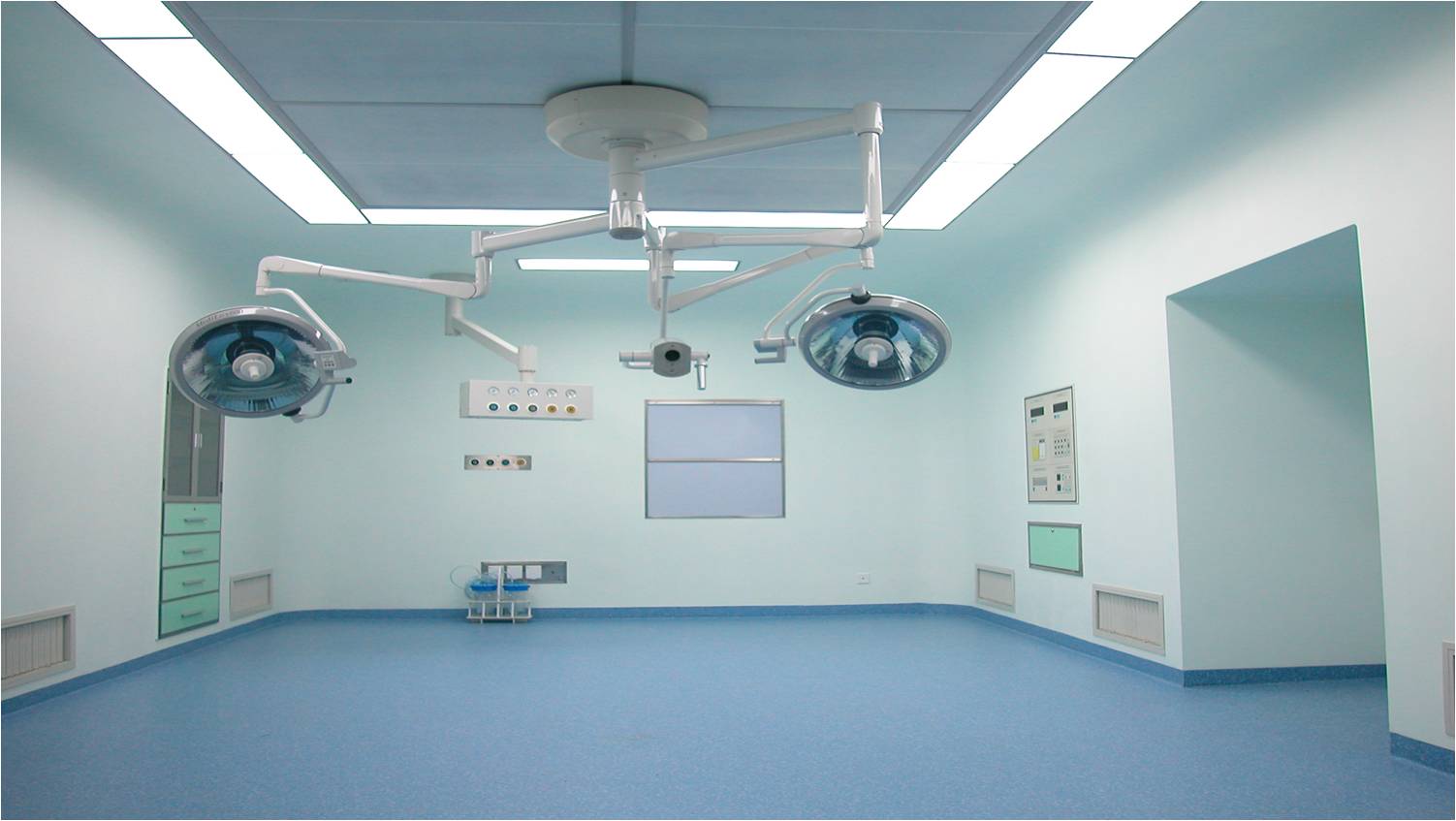
一、 實驗室建設原則細胞實驗室的建設,旨在創造一個安全、有效、符合科學研究要求的實驗環境。實驗室應滿足細胞研究、制備、培養、檢測等全過程的需求,確保各項實驗活動能夠順利進行。嚴格遵守生物安全法規,采取嚴格的安全措施,防止生物污染、交叉污染和實驗事故的發生。根據實驗需求,設定不同級別的潔凈區域,確保空氣質量和環境衛生,以保障實驗結果的準確性和可靠性。實驗室設計應具有一定的靈活性,以適應未來科研方向和技術發展的變化。二、空間布局設計將實驗室劃分為不同的功能區域,如樣品接收區、樣品處理區、細胞培養區、檢測區、廢物處理區等。各區域之間應有明顯的分隔和標識,以避免污染。設計合理的人員和物流通道,確保實驗人員、樣品和物資的流動有序且互不干擾。潔凈區與非潔凈區則根據實驗需求劃分潔凈區和非潔凈區, 并采取相應的凈化措施。潔凈區應嚴格控制人員進出,減少污染。三、環境控制設計安裝高效過濾器(如HEPA過濾器)和送排風系統,確保實驗室內的空氣潔凈度達到要求。定期檢查和更換過濾器,以保證其過濾效率。安裝溫濕度傳感器和控制系統,保持實驗室內溫濕度穩定。根據實驗需求設定合適的溫濕度范圍,以提高細胞培養的效率和穩定性。提供充足的照明和良好的通風條件,確保實驗 人員的舒適度和實驗操作的準確性。照明設備應易于清潔和維護,避兔積塵和污染。四、設備配置與選型基礎設備包括生物安全柜、超凈工作臺、離心機、顯微鏡等...
發布時間:
2025
-
01
-
02
瀏覽次數:19
一、粉針分裝劑的工藝要求粉針分裝劑藥品,由于所生產的藥品通常是對熱處理敏感,不耐溫,不適合采用最終滅菌,只能使用非最終滅菌的無菌操作工藝。分裝產品一般為抗生素產品,對于抗生素類產品,國家有著嚴格的特殊規定。根據GMP規范規定,生產抗生素類藥品必須使用獨立的廠房與設施,空調系統的排氣應經凈化處理,排放的廢氣不得含有該類藥品的塵粒,以上生產區域的排風口應盡可能遠離其他藥品生產區域空氣調節系統的進風口。二、粉針分裝車間工藝設計考慮的幾個要點1.污染物控制措施(1)人員的凈化:操作人員是潔凈室中最主要的污染源之一,因此為了減少人員的污染,進入潔凈室的人員必須凈化。人員凈化室應根據產品生產工藝和空氣潔凈度等級要求布置,出入非無菌潔凈區、無菌潔凈區的人員凈化程序分別按GMP規范規定的要求來進行。需要強調的是,現在好多企業粉針劑車間的無菌潔凈區的人員更衣,只是從非無菌潔凈區經過更衣室、緩沖區進入無菌潔凈區,這不是很合理的。進入無菌室內的工作人員要經過嚴格的洗滌消毒處理程序以后才能夠進入無菌操作區。最好對無菌區單獨設立獨立的更衣系統,不要經過非無菌區,以免.非無菌區影響無菌區。另外,由于粉針分裝大多是抗生素類產品,更衣系統必須設置淋浴室。(2)物料的凈化:物料通常指原料、輔料、包裝材料等。這里也包含蓋膠塞、西林瓶等進入潔凈區的其它物品。一般而言,物料進入潔凈區前,需要在外包裝清潔室對外包裝進行必要...
發布時間:
2024
-
12
-
31
瀏覽次數:26
一、原料藥車間的主要特點1.反應過程復雜,操作工序繁多,部分反應條件苛刻。例如,反應過程會有副反應以及中間產物等,有些反應需要在高溫高壓條件下進行。2.使用大量易燃易爆的有機溶劑、酸、堿以及有毒害物質等,車間對防火、防爆.防腐的要求較高。原料藥車間常用溶劑甲醇、甲苯、乙醇、鹽酸、液堿。3.設備數量和種類較多,管道種類和數量大;原料藥車間涉及反應釜(搪玻璃、不銹鋼)、儲槽、固液分離(離心機、過濾器)干燥(雙錐真空干燥、噴霧干燥)、冷凝器(螺旋板、螺旋纏繞、列管)、真空泵(無油立式、羅茨真空泵)、輸送泵等設備。4.要充分考慮危險工藝和使用特殊物料工藝布置(例如需要隔房間,獨立的通排風等)。5.盡量利用位能考慮物料的輸送(高位槽、固體投料),以節約能耗、縮短管道等。6.原料藥精烘包(精制、烘干、包裝)崗位要按照GMP要求(潔凈區的生產以及精烘包的泄爆等)。二、原料藥車間布置原則1.車間布置以滿足工藝生產要求為前提,以工藝流程為基礎,從利于生產操作和便于生產管理的角度出發,合理進行功能性區域劃分及設備布置設計。2.車間布置應滿足安全.環保及職業衛生的要求。具體而言,在第一個原則上,要順應工藝流程布置,上下縱橫相呼應,確保水平方向和垂直方向的連貫性,盡量縮短物料運輸路線,節約能源;相同設備或同類設備、性質相似及聯系密切的設備相對集中布置,以便于集中管理、統一操作;設備垂直方向布置不僅要充分考...
發布時間:
2024
-
12
-
30
瀏覽次數:15
一、原料藥多功能車間的基本概念原料藥多功能車間不同于傳統的原料藥車間,它可以同時或分期生產不同品種的多種原料藥。這些原料藥之間需要有一定的相似性,例如:具有相近的生產工藝、所用的設備多數可以通用等等。多功能車間的建設可以滿足小批量、多品種的生產要求,應對市場的迅速變化。二、原料藥多功能車間的通用工藝流程大多數原料藥的生產過程可分為五大部分:(1)一步或幾步化學反應;(2)粗品結晶、固液分離;(3)精制即粗品溶解、脫色、過濾、重結晶;(4)成品干燥包裝;(5)“三廢”的后處理。其中第①部分即合成部分,可由多個合成單元組合而成;第③、④部分位于凈化區內。因此,原料藥多功能車間的生產流程可系統化為:反應、精制、分離、干燥、包裝。三、原料藥多功能車間的設備布置原料藥多功能車間內的設備布置與普通原料藥車間的設備布置有許多相同之處,如:設備布置要滿足水平和垂直方向的連續性;要充分利用位差使物料自動流送,避免物料過多的往返于樓層之間;設備排列盡量整齊,要留有足夠的操作及檢修空間;需要滿足GMP要求等。設備布置除了這些與普通原料藥車間相同之處外,還要滿足多功能車間的特殊要求,在設計時必須考慮以下原則:(1)適當預留擴建余地,一般每隔3~4個操作單元預留一個空位,以便以后更換產品時增加相應的設備。(2)必須考慮設備檢修、拆卸所需的起重運輸設備,如果不設永久性的起重運輸設備,則應有安裝起重運輸設備的場...
發布時間:
2024
-
12
-
28
瀏覽次數:17
根據人體健康素質完善要領和安全生產標準分析,尤其是口服固體藥劑,在秉承外部環境有效隔離的指標前提下,全力避免階段瓶頸限制的擴散效應。藥品內部活性成分是無法做到徹底消除的,因此對于現場布置員工多少會造成一定的危害.在此條件下制藥企業完全有必要在遵守法令條文規定的基礎上,采取額外措施進行綜合補救并借此穩定產業靈活驅動效應。一、粉塵處理的現實意義論述制藥廠整體活動布置的中心指標就是維持產品的保護功能實效,透過必要的隔離設備和設計標準,將內部生產區域與外部人員、生態環境做出有效隔離,減少額外效應衍生的環境污染和人員健康危害問題。目前現代化智能控制技術不斷發達,有關這部分保護理念就更加深刻了,無論任何模式的保護方案,大體上還是圍繞粉塵隔離處理的動機需求進行相應的裝置設計。二、粉塵科學隔離與綜合處理的滲透模式探析現實制藥廠在不得已的條件下,往往要進行規模化的有毒制品生產,在相關替代物質和工藝條件不夠齊全的狀況下,唯一的切入點就是現場工序環節與生態環境的隔離化處理。對于口服固體藥劑生產線控制工作來說,其主體職責就是將物料輸送和藥品生產流程中的粉塵做出合理處理。(一)隔離等級的確認在某種物料實際暴露危害限度確定的情況下,有關方案規劃人員就有必要聯合現場環境隔離等級進行科學認證,并從中選取相匹配的應對方案,此類方案格式存在兩類,首先是處于隔離化形態的設備模型,其次是相應的廠房構架規劃。(二)口服固體...
發布時間:
2024
-
12
-
27
瀏覽次數:16
在疫苗的生產企業在生過程中會產生大量的活毒廢水,廢水中肯定含有部分活著的細菌和病毒,按照相關的環保法規和GMP要求,這些廢水必須要嚴格處理,達到無害化要求才能排放。滅活系統的工作原理:生物活毒廢水滅活系統中使用高溫高壓蒸汽對活毒廢水進行直接加熱和間接加熱的方式,在持續高溫的狀態下對廢水中的活毒進行消殺。這種滅活方式可以消殺廢水中的病毒和活菌。而且結構簡單,適合大噸位的生產。在已投產的設備中對滅菌性能進行檢驗、檢測和驗證,總結了滅菌設備先進的設計理念、安全保障,為醫藥和生物制品生產的安全有效性提供科學依據。驗證結果表明:高壓蒸汽滅菌運行周期短、安全性能強、滅菌質量穩定可靠。生物活毒廢水滅活系統是高效的滅菌裝置,根據用戶的廢水產量的多少,系統可采用連續和間歇的工作方式。根據用戶提供的數據設計收集罐和滅活罐的容積。在生產和實驗過程中,車間活毒廢水通過廢水收集池集中儲存,收集池設計容量為20T,當廢水池的容量達到一定標準(設定液位標準可調(0-4m),項目根據生產車間平均排水量,設置的液位參數為+2.0m,此時收集池廢水儲量為10T),收集池液位計向PLC柜發送型號,自吸泵(一用一備)啟動工作,將廢液輸送至滅活罐,輸送管道采用304不銹鋼,設置止回閥和聯接有蒸汽滅菌裝置。滅活罐采用壓力容器設計,罐體304不銹鋼材質,并設置有排氣管和保溫夾套。滅活罐容量到達設計值,自吸泵停止工作,閥門關閉,...
發布時間:
2024
-
12
-
26
瀏覽次數:18
固體制劑在生產時,需要粉碎→制粒→總混→壓片→充填單元→物料轉運等,在每個環節都易產生粉塵,進而導致污染和交叉污染,從而降低藥品質量。為有效的降低粉塵情況,可采用新型工藝設備以及封閉物料進行轉運方式,達到提高產品質量的目的。一、制粒生產聯動線固體制劑聯動生產線是由包衣機、沸騰干燥機、移動提升機、濕法混合制粒機、固定提升整粒轉料機、料斗提升加料機等設備構成。其中濕法混合制粒機中有真空上料功能,包含連續式和間歇式真空上料,用真空源通過缸蓋上端的過濾器把料缸抽空之后產生負壓從而實現真空上料,上料結束將真實閥關閉,排空閥打開并且開啟設備,物料通過切線式攪拌槳的作用,將料缸中心逐漸推向料缸邊緣,接近缸壁之后,受力方向更改導致物料沿著缸壁提升,產生充分流化,當上升的物料達到椎體位置時,受力方向會隨著椎體角發生變化,回到缸體中間位置,并且再次進行下一個運動過程。沸騰干燥機利用自身所產生的負壓,將濕顆粒送入到料倉內,上料完畢后, 將進料閥關閉實施干燥,空氣通過初效、中效、高效過濾以及熱交換器之后,輸送到料倉底部,把物料吹起來達到沸騰的效果,同時設定好進風溫度,從而實現冷熱空氣補償的情況,沸騰艙內的物料受到熱風作用下,使物料中的水分逐漸增發,腔體內的補足帶會根據設定程序實施交替抖動,從而預防堵塞情況凹。補足帶在抖動過程中,排風閥要關閉,是粘附在補足帶的物料可以抖落下來,在操作過程中,一定要確保補足帶...
發布時間:
2024
-
12
-
25
瀏覽次數:24
對于一個制藥車間或廠房的設計,首先應整體考慮建筑物的位置、人、物流出入口、工藝流程的合理性、空間平面的利用率、節能生產等問題,同時應協調好工藝與建筑、消防、空調、動力等之間的關系。在滿足生產要求的前提下,盡量減少潔凈區(特別:是無菌區)的面積以降低能耗。另外,還要考慮生產的機械化、自動化,盡量減少人員操作,把對產品的污染風險降至最低。下面以某脊灰減毒活疫苗生產車間為例,從以下幾個方面對其工藝平面設計進行分析。一、工藝區劃方案根據脊灰疫苗生產工藝各工序的特殊要求及相互關系,利用縱橫走廊將生產車間分設7個功能區:生產區分為細胞區(無毒區、C級、局部A級區)、病毒區(有毒區、C級、局部A級區)、配苗區(有毒區、B級、局部A級區)、分裝區(有毒區、B級、局部A級區)、外包裝區(無毒區、K級區);由于在生產過程中的細胞培養、細胞種毒后培養需要大量的細胞培養液,因此,在車間內設置一個單獨的配液區(無毒區、D級區),進行培養基的配制;每個生產區使用的大量的器具需要進行回洗、滅菌后重復使用,因此,車間還需設置統一的清洗區(無毒區、D級區)。每一工作區設置獨立的人、物流出入口,并同其他區域嚴格分開。二、人、物流設計新版GMP多次強調了避免混淆及交叉污染的問題,因此在進行生物制品類廠房設計時應考慮將人、潔物、污物分開。車間分別設計人流入口、物流入口以及污物出口。人流從廠房東北側門廳進入,經換鞋、更衣進...
發布時間:
2024
-
12
-
24
瀏覽次數:20
一、防火分區設計要點電子潔凈廠房防火分區的劃分,應該滿足以下要求:1)對于甲、乙類潔凈廠房,最好設計為單層,且單層廠房防火分區的最大允許建筑面積宜為3000m2,而多層廠房宜為2000m2;2)對于丙、丁、戊類潔凈廠房,其防火分區的最大允許建筑面積應該滿足《建筑設計防火規范》中的有關要求;3)根據電子工業潔凈廠房設計規范的相關規定,對于耐火等級為一、二級的丙類電子工業潔凈廠房,如凈化空調回風氣流中安裝有靈敏度不低于0.01%obs/m的極早期煙霧探測裝置,則每個防火分區的最大允許建筑面積可根據具體的生產工藝要求來予以確定。二、疏散方面設計要點電子潔凈廠房的安全疏散設計主要涉及安全出口、疏散走道疏散樓梯等。在疏散距離設計上,考慮到電子潔凈廠房本身的特點,應在設計時充分考慮人員疏散的要求,全面分析疏散人流、疏散距離等因素,并經過嚴格的模擬和計算,得出最佳疏散路線,同時對于安全出口及疏散通道的布置也要進行合理規劃,使生產地點與安全出口之間搭建起便捷、暢通的逃生路線,而不必經過曲折的凈化路線。在《電子工業潔凈廠房設計規范》中,針對其工藝特點,疏散設計也提出了特別的要求。三、電氣化方面設計要點1)電源方面潔凈廠房凈化空調系統的用電負荷、照明負荷應由變電所專線供電。消防用電設備的供配電設計應按現行國家標準規定執行。電源進線(不包括消防用電)應設置切斷裝置,并盡量設在潔凈區外便于管理的地點。潔凈...
發布時間:
2024
-
12
-
23
瀏覽次數:18
重組疫苗是指采用基因重組技術將編碼病原微生物保護性抗原的基因重組到細菌、酵母或細胞,經培養、增殖后,提取、純化所表達的保護性抗原制成的疫苗"。重組疫苗生產技術作為現代生物科學領域中的重要進展,具有安全性好、生產周期短、易于放大生產,是當今與未來疫苗研制與開發的主要方向之一。重組疫苗生產工藝具有生產周期長、生物安全風險高以及生產過程控制嚴格等特點。針對重組疫苗生產工藝特性,結合GMP和相關設計規范,開展重組疫苗GMP車間設計要點分析具有重要意義。一、工藝流程設計重組疫苗的典型生產工藝流程大致分為三個階段:(1)上游(從種子復蘇到澄清):種子復蘇擴增,在種子罐擴增后,在發酵罐/生物反應器進行批培養。原核表達體系經細胞破碎,澄清,進入下游工藝,真核表達體系經過澄清,收獲液進入下游。(2)下游(從層析到原液):收獲液經過不同類型的層析柱,去除其中的蛋白碎片、DNA等,經超濾濃縮,獲得精純產物,加入佐劑制得原液。(3)制劑(從原液到成品人庫):原液經制劑分裝-燈檢-包裝得到成品,送至2~8℃庫中保存。重組疫苗的制劑型式有:預灌封水針、西林瓶水針、凍干等。二、車間布置設計1.車間布置主要遵循的標準規范《藥品生產質量管理規范( 2010年修訂)》;GB 50016- -2014《建筑設計防火規范》( 2018年版);GB 50073- -2013《潔凈廠房設計規范》;GB 50457-...
發布時間:
2024
-
12
-
21
瀏覽次數:26
回到頂部
 瀏覽手機網站
瀏覽手機網站 賽特公眾號
賽特公眾號分享到:
總部地址:廣州市天河區粵墾路611號力達廣場
TEL : 020-38090335 38090330 FAX : 020-38090326
郵箱:guangzhou@stpurify.com
TEL : 020-38090335 38090330 FAX : 020-38090326
郵箱:guangzhou@stpurify.com
生產基地:廣東省潮州市潮安區東鳳禮陽李工業區
TEL:0768-6585795 6581475 FAX:0768-6582900
郵箱:st@stpurify.com